Eigenschaften von Säuren
Täglich kommen wir mit Säuren und Basen in unserem Alltag in Kontakt, da diese z.B. in Lebensmitteln oder Reinigungsmitteln enthalten sind. Je nach Konzentration und Anwendung verfügen sie über unterschiedliche Eigenschaften. Säuren können z.B. ätzend wirken. Das bedeutet, dass sie in Kontakt mit anderen Stoffen chemische Reaktionen auslösen können. Dies hat zur Folge, dass sich neue Stoffe bilden und/oder chemische Strukturen von Stoffen zerstört werden. Wir interessieren uns vor allem für Reaktionen, bei der Säuren in Wasser gelöst werden und sich eine saure Lösung bildet.

- Schau dir die Präsentation an.
Merke dir den Fachbegriff: Dissoziation
Der Vorgang der Dissoziation beschreibt das selbstständigen Aufspaltung eines Stoffes in zwei oder mehrere Atome, Moleküle oder Ionen, wie es bei Säuren in Wasser der Fall ist.
Eigenschaften von Basen
Nachdem wir uns nun mit Säuren beschäftigt haben, können wir uns den Basen widmen. Wie schon bei den Säuren sind für uns vor allem die Reaktionen interessant, die in Wasser ablaufen. Aus diesem Grund sprechen wir auch von basischen Lösungen. Basische Lösungen werden auch als Laugen bezeichnet. Wie eine Lauge entsteht, werden wir uns noch lernen. Wie auch schon die Säuren verfügen Laugen ebenfalls über eine ätzende Wirkung und können bei Kontakt mit der Haut zu schweren Verletzungen führen. Die folgende Abbildung zeigt uns verschiedene Reaktionen von Laugen.

- Schaue dir die Präsentation an.
Säure-Base-Definition nach BRONSTED
Wir haben nun schon das Grundprinzip einer Säure-Base-Reaktion anhand von Beispielen kennengelernt. Jedoch war es historisch gar nicht so einfach, eine Definition für eine Säure-Base-Reaktion zu finden. Zahlreiche Wissenschaftler haben sich daran versucht und unterschiedliche Vorschläge entwickelt. Jedoch mussten die Vorschläge mehrfach weiterentwickelt werden. Eine immer noch gültige Definition ist die von Brønsted und Lowry:
Säuren sind Protonendonatoren und Basen sind Protonenakzeptoren.
Die beiden Chemiker BRONSTED und LOWRY machten 1923 unabhängig voneinander den Vorschlag, dass Säuren Protonen (H+) abgegeben und Basen Protonen (H+) aufnehmen. Dieser Vorgang wird auch als Protolyse bezeichnet und beschreibt die Protonenübertragung einer Säure-Base-Reaktion.
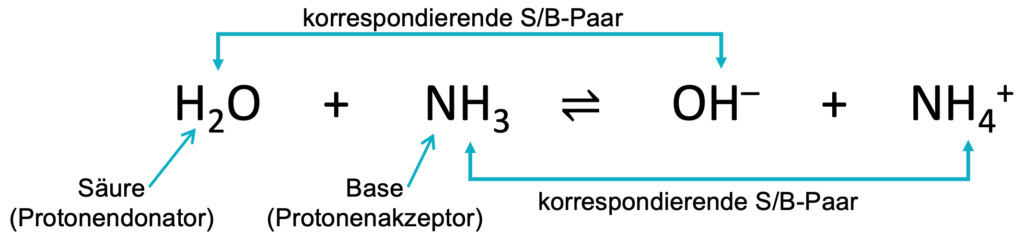
Eine Säure-Base-Reaktion (S/B-Reaktion) kann nur ablaufen, wenn beide Teilnehmer vorhanden sind. Daher stehen Säuren und Base miteinander in Beziehung. Außerdem gibt es S/B-Reaktionen, die in beide Richtungen ablaufen können. Dies wird durch den Doppelpfeil (⇌) dargestellt. Verdeutlichen wir uns das an dem dargestellten Beispiel: Die Säure (H2O) wird, nachdem sie das Proton abgegeben hat, zur korrespondierenden Base (OH–). Aus der Base (NH3) bildet sich (nach der Protonenaufnahme) die korrespondierende Säure (NH4+).
- Übertrage die angegebenen Reaktionsgleichungen in der Präsentation in deine Unterlagen und umkreise auf beiden Seiten der Reaktionsgleichungen mit unterschiedlichen Farben die Säuren bzw. Basen und hebe mit einem Pfeil das korrespondiere S/B-Paar hervor.
- Tippe auf das Symbol hinter der Reaktionsgleichung, um die Lösung anzuzeigen. Aber erst selber lösen! 😉
Zeit für eine Zwischensicherung der gelernten Inhalte
Universalindikator und der pH-Wert
Nicht jede Säure oder Base ist gleich ätzend und wenn wir zu einer sauren oder basischen Lösung sehr viel Wasser geben, verringert sich ihre Wirkung. Es gibt also Unterschiede und diese Unterschiede haben einen Einfluss auf andere Reaktionen. Wir müssen also einen Weg finden, um die Vielfalt von sauren oder basischen Lösungen beschreiben zu können.
Eine Möglichkeit wäre mit Säure-Base-Indikatoren (S/B-Indikator) zu arbeiten. Ein S/B-Indikator zeigt dir bestimmte Informationen einer chemischen Lösung an und dient damit als Hilfsstoff. Ändert sich der Zustand einer Lösung wird dies durch einen Farbwechsel angezeigt. Ein S/B-Indikator besteht aus verschiedenen Farbstoffen. Wir haben die Wirkung von sauren oder basischen Lösungen auf einen Farbstoff bereits kennengelernt. Einer der aussagekräftigsten Indikatoren ist der Universalindikator.
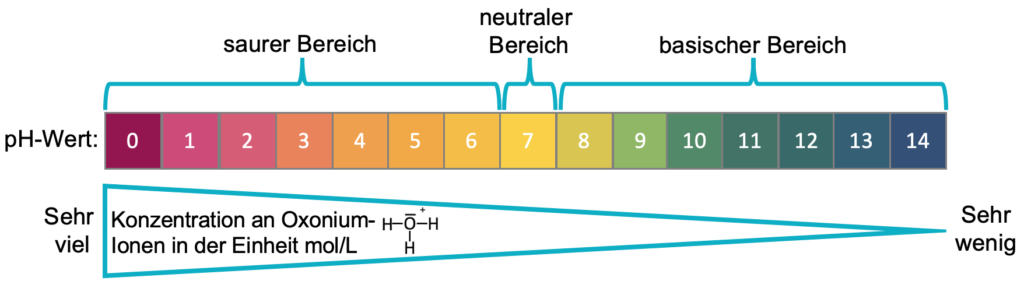
Du kannst aus der Abbildung ablesen, dass die Farbskala in drei Bereiche eingeteilt ist, die wiederum aus weiteren Farbabstufungen besteht. Wir erinnern uns, dass bei der Zugabe einer Säure in Wasser Oxonium-Ionen (H3O+-Ionen) entstehen. Je höher die Konzentration, desto saurer ist eine Lösung. Um zu beschreiben, wie sauer eine Lösung ist, wurde der pH-Wert eingeführt. Der pH-Wert ist ein Maß dafür, wie sauer oder basisch eine Lösung ist und dieser lässt sich aus der Konzentration der Oxonium-Ionen berechnen.
Der pH-Wert lässt sich in einer pH-Wert Skala von 0 bis 14 unterteilen und dieser entspricht genau den dargestellten Farbabstufungen. Der pH-Wert 0 ist ganz links und beschreibt einen sehr sauren pH-Wert, während der pH-Wert 14 einen sehr basischen pH-Wert beschreibt.
pH = -log [Oxonium-Ionen] oder gängiger ist pH = -lg [H3O+]
Ich hoffe die Definition des pH-Wertes erscheint dir nicht zu kompliziert. Das ist nämlich recht einfach: „-lg“ bedeutet der negative dekadische Logarithmus. Dabei handelt es sich um eine Taste auf deinem Taschenrechner und die eckigen Klammern [ ] bedeuten, dass du dort die Konzentration der H3O+-Ionen einsetzen sollst und dann erhältst du den pH-Wert.
Wir machen ein Beispiel: In einer sauren Lösung entspricht die Konzentration der Oxonium-Ionen 1 mol/L.
pH = -lg [H3O+] ➔ pH = -lg 1 mol/L = 0
Damit haben wir einen pH-Wert von 0. Ganz einfach, oder? 😉
Vertiefung: Was bedeutet der Begriff „Mol“ bzw. „mol/L“
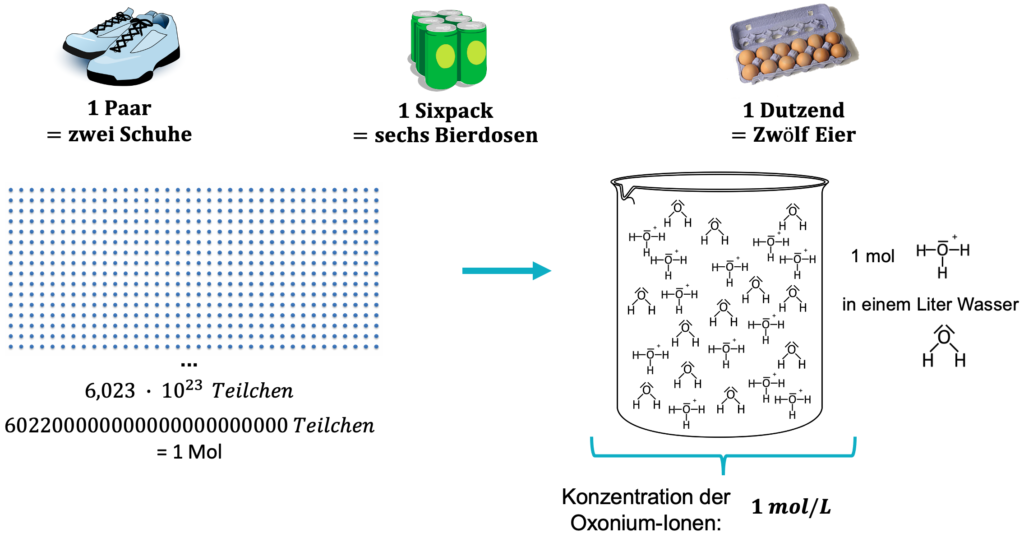
Die Anzahl der Teilchen (Atome, Moleküle oder Ionen) in einer Lösung ist sehr groß, wir bewegen uns nicht in einer Größenordnung von 5-500 Teilchen, sondern in einer Größenordnung von 602200000000000000000000 Teilchen. Das ist eine seeehr große Zahl. Aus diesem Grund hat man sich in der Chemie auf eine neue Einheit geeinigt: Das Mol.
Man fasst diese seeehr große Zahl einfach zusammen und legt fest, dass mit 1 mol eine Teilchenzahl von 602200000000000000000000 gemeint ist.
Ich bin mir sicher, dass hast du im Alltag schon mal gemacht. 1 Paar Schuhe entsprechen auch 2 einzelnen Schuhen oder ein Sixpack-Bier entspricht 6 einzelnen Flaschen und dieses Prinzip wenden wir in der Chemie auch an. Angenommen wir haben 1 Liter einer sauren Lösung, in der sich 1 mol Oxonium-Ionen befinden. Dann haben wir eine Konzentration von 1 mol/L. Anders ausgedrückt, in der Lösung befinden sich 602200000000000000000000 Oxonium-Ionen in einem Liter.
- Beantworte die Fragen in dem Quiz.
Neutralisation von Säuren und Basen
Wir haben im Abschnitt Basen bereits erkennen können, dass eine saure und basische Lösung sich neutralisieren können. Bei diesem Vorgang entsteht Salz. Ganz allgemein können wir festhalten: Säure + Lauge -> Salz + Wasser
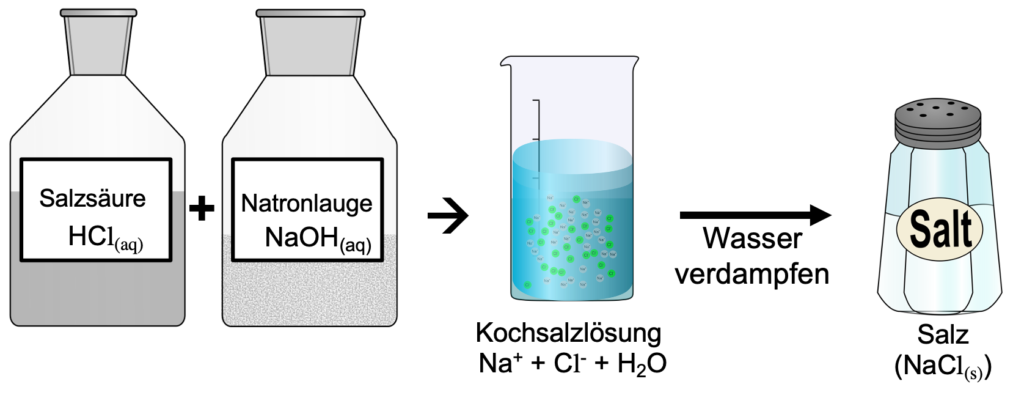
Die Abbildung verdeutlicht die Neutralisation am Beispiel von Natronlauge und Salzsäure:
HCl(aq) + NaOH(aq) -> NaCl(aq) + H2O
Aus dieser Reaktionsgleichung gehen jedoch nicht alle an der beteiligten Stoffe hervor. Das liegt daran, dass die Reaktion gelöst in Wasser abläuft. Dies können wir an dem Tiefgestellten (aq) erkennen. Als nächstes können wir die Ionengleichung für die Neutralisation unter Berücksichtigung der Dissoziation in Wasser aufstellen:
Na+ + Cl– + H3O+ + OH– -> Na+ + Cl– + 2 H2O
Aus der Reaktionsgleichung können wir ableiten, dass bei einer Neutralisation die H3O+ und OH–-Ionen miteinander reagieren, indem ein Proton (H+) vom H3O+ auf das OH–-Ion übertragen wird. Dieser Vorgang ist bei jeder Neutralisation identisch, egal um welche Säure oder Base es sich handelt.
Die Na+ – und Cl– -Ionen verbleiben in der Lösung und können durch Verdampfen des Wassers festes Salz (Natriumchlorid) bilden, dass über Ionenbindungen zusammenhält.
- In der Präsentation werden verschiedene Neutralisationsreaktionen dargestellt.
- Stelle die Ionengleichungen für die einzelnen Neutralisationen auf.
Erklärvideo zum Thema Säuren und Basen
Das Wissen zum Thema Säuren und Basen gehört zu den wichtigen Grundkenntnissen der Chemie. Aus diesem Grund habe ich die wichtigsten Inhalte noch einmal in einem Erklärvideo für euch zusammengefasst.
- Schaue dir das Erklärvideo an.
- Halte das Video nach 8. Minuten an und überprüfe dein Wissen mit Hilfe der beiden interaktiven Übungen:
- Überprüfe dein Wissen am Ende des Videos, mit den beiden folgenden interaktiven Übungen:
Das wichtigste auf einem Blick