Das „Johnstone-Dreieck“
In der Chemie können wir Stoffe und chemische Reaktionen beobachten, aber auch auf weiteren Ebenen darstellen und beschreiben. Das folgende Dreieck verdeutlicht die möglichen Ebenen. Wir können ein Becherglas mit etwas Wasser als klare durchsichtige Flüssigkeit beobachten (makroskopische Ebene). Wir können die Flüssigkeit auch beschreiben, indem wir statt dem Begriff „Wasser“ die Schreibweise „H2O“ (symbolische Ebene) wählen. Eine weitere Möglichkeit wäre, wir nutzen Modelle, die uns eine räumliche Vorstellung der einzelnen Atome und Moleküle durch Kugeln ermöglichen (submikroskopische Ebene).
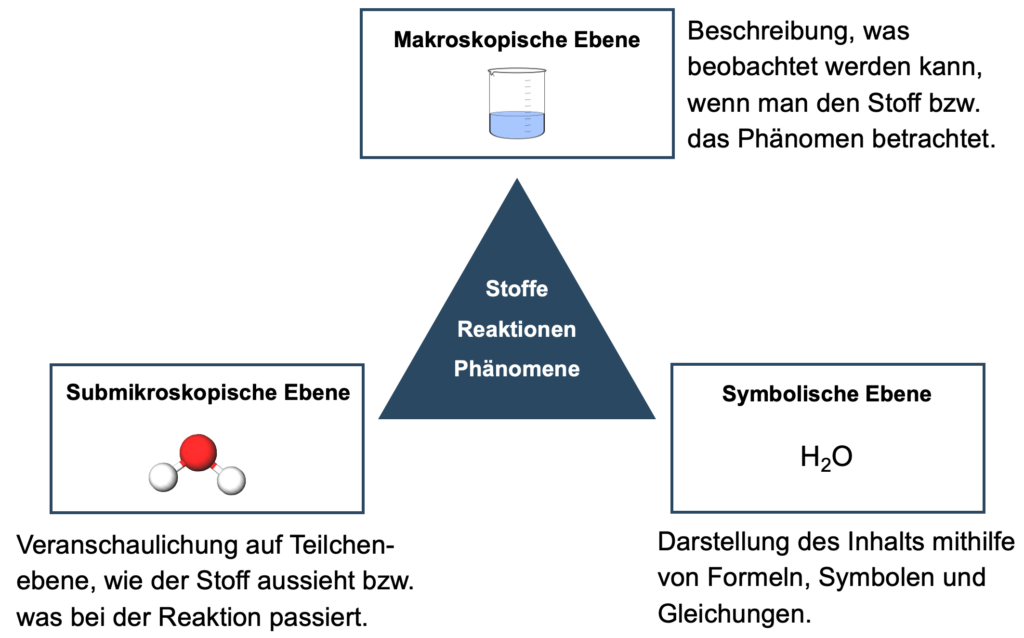
Dieses Dreieck wird auch nach seinem Erfinder Johnstone benannt. Er stellte fest, dass im Chemieunterricht häufig Verständnisprobleme entstehen, wenn die verschiedenen Ebenen miteinander vermischt werden. Um diese besser auseinanderhalten zu können, veröffentlichte er ein Modell, das unter dem Namen „Johnstone-Dreieck“ sehr bekannt wurde.
- In der folgenden Übungen werden dir verschiedene Darstellungsmöglichkeiten aus der Chemie gezeigt. Ordne den Abbildungen eine Ebene aus dem „Johnstone-Dreieck“ zu.
- Schaue dir das Video zur Knallgasreaktion an. Bei einer Knallgasreaktion reagiert Wasserstoff mit Sauerstoff zu Wasser.
- Beschreibe den Ablauf der Knallgasreaktion mit den drei Ebenen aus dem „Johnstone-Dreieck“ in der folgenden Reihenfolge (makroskopische, submikroskopische und symbolische Ebene).
Der Begriff Stoff in der Chemie
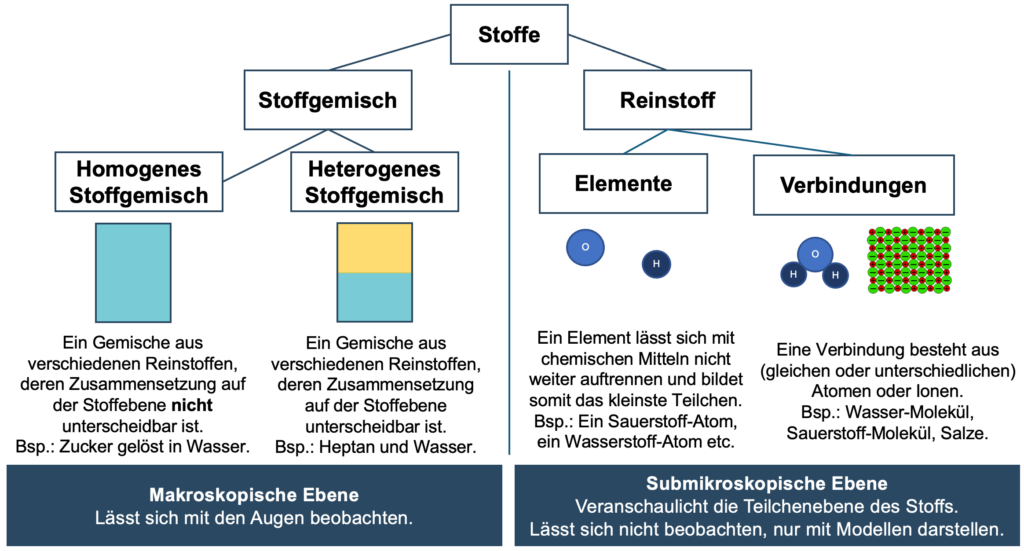
In der Chemie wird auch häufig der Begriff Stoff oder Stoffe verwendet. Genauer müsste man von chemischen Stoffen sprechen. Ein Stoff lässt sich beobachten, untersuchen und besitzt eine Masse. In der folgenden Abbildung kannst du erkennen, dass sich der Begriff noch weiter unterteilen lässt. Ein Beispiel für ein Stoff wäre Wasser. Genauer handelt es sich um einem Reinstoff, da dieser nur aus Wassermolekülen (H2O) besteht. Ein anderes Beispiel für einen Reinstoff wäre Zucker bestehend aus Glucose-Molekülen (C6H12O6).
Werden diese beiden Stoffe miteinander vermischt, spricht man von einem homogenen Stoffgemisch, da beide Stoffe ineinander gelöst und nicht unterscheidbar sind.
Außerdem kann zwischen der makroskopischen und submikroskopischen Ebene unterschieden werden. Wir können mit unseren Augen ein homogenes Stoffgemisch betrachten und auf der submikroskopischen Ebene können wir mit Teilchenmodellen das Stoffgemisch beschreiben.
Aufstellen und Ausgleichen von Reaktionsgleichungen
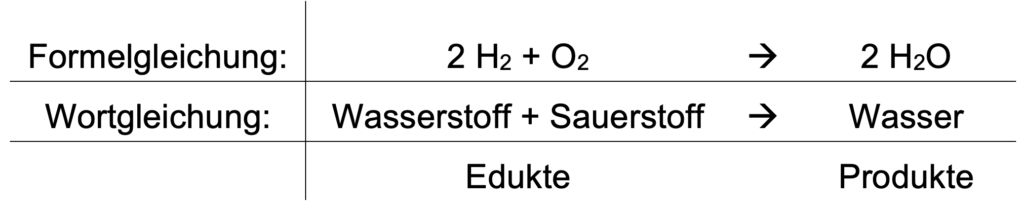
Mit Hilfe einer Formelgleichung lässt sich eine chemische Reaktion mit Hilfe der Symbolschreibweise darstellen. Dabei reagieren Edukte zu Produkten. Aus der nachfolgenden Tabelle geht hervor, dass eine Reaktionsgleichung immer aus Edukten, einem Reaktionspfeil (→) und Produkten besteht. Demnächst werden wir noch einen weiteren Reaktionspfeil (⇌) kennenlernen, der verdeutlicht, dass Reaktionen in beide Richtungen verlaufen können.
Bei einer Reaktionsgleichung ist zu beachten, dass links und rechts des Reaktionspfeils die gleichen Atome in der gleichen Anzahl stehen, auch wenn sie unterschiedlich miteinander verknüpft sind. Erst wenn das zutrifft, ist eine Reaktionsgleichung ausgeglichen.
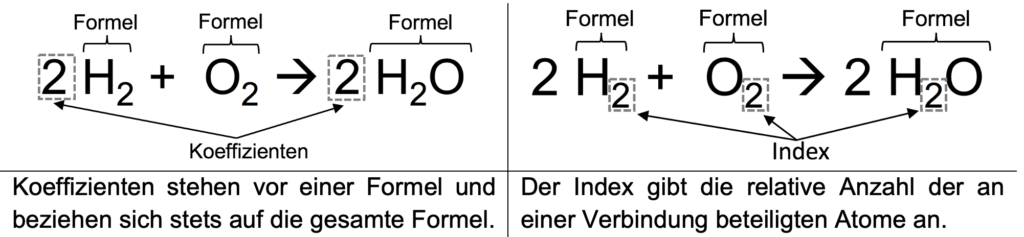
In der folgenden Abbildung können wir erkennen, dass an verschiedenen Stellen Zahlen auftauchen. Diese Zahlen lassen sich als Koeffizienten und Indices benennen. Der Index gibt an, wie oft ein Atom im Moleküle vorkommt, während der Koeffizient sich auf die gesamte Formel bezieht. Mit dem Koeffizient wird auch ausgedrückt, wie oft ein Molekül in der Reaktionsgleich vorkommt.
- Wähle die korrekte Reaktionsgleichung aus und notiere diese in deinen Unterlagen.
Redoxreaktionen
Übertragung von Elektronen während einer chemischen Reaktion
Damit eine chemische Reaktion ablaufen kann, müssen die Edukte in Kontakt kommen. Bei den meisten chemischen Reaktionen werden Elektronen von einem Atom auf ein anderes übertragen. Damit muss ein Atom Elektronen abgeben (Fachbegriff: Oxidation) und ein anderes Atom diese Elektronen direkt wieder aufnehmen (Fachbegriff: Reduktion). Dieser Vorgang wird als Redoxreaktion bezeichnet.
Merke
Oxidation ist die Abgabe von Elektronen, Reduktion die Aufnahme von Elektronen. Redoxreaktionen sind Elektronenübertragungsreaktionen.
An einem Beispiel wollen wir uns eine Redoxreaktion veranschaulichen. Dazu wird Magnesium mit Sauerstoff verbrannt (Ein Video zu dem Versuch gibt es auf Youtube – hier klicken).
Die folgende Abbildung zeigt die Reaktionsgleichung zu dem Versuch. Die Magnesium-Atome (Mg) geben ihre Elektronen ab, damit werden sie als Elektronendonatoren bezeichnet. Die Sauerstoff-Moleküle (O2) werden in ihre Atome gespalten, dies kann nur funktionieren, wenn sie Elektronen aufnehmen. Die Sauerstoff-Moleküle werden auch als Elektronenakzeptoren bezeichnet. Durch dieses Vorgang entsteht ein neues Produkt das Magnesiumoxid (MgO).
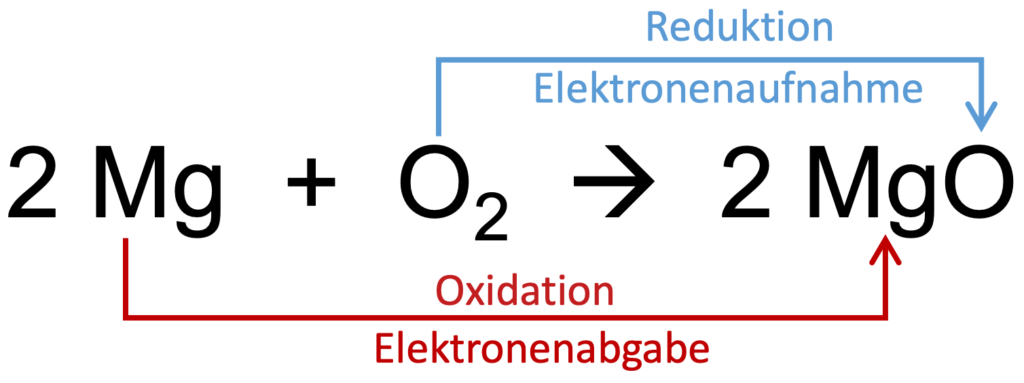
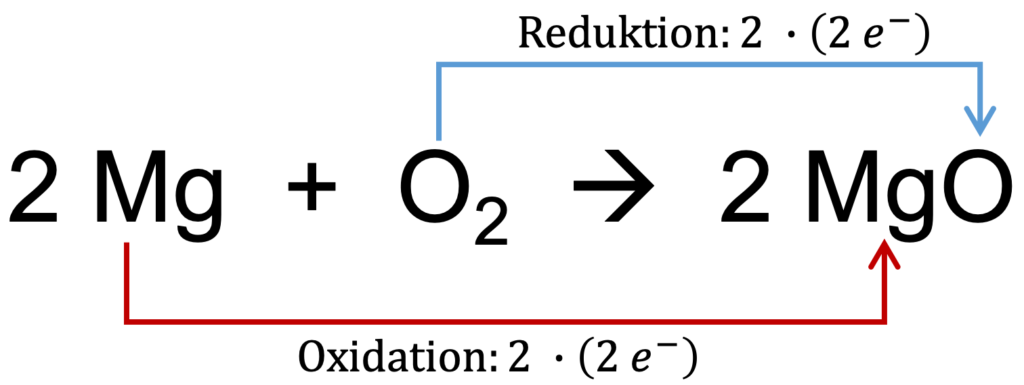
Auf der rechten Seite der Abbildungen kannst du erkennen, dass hinter den Begriffen Oxidation und Reduktion auch die Anzahl der Elektronen steht, die abgegeben bzw. aufgenommen werden. Insgesamt geben die Magnesium-Atome 4 Elektronen ab, während das Sauerstoff-Molekül die 4 Elektronen aufnimmt.
Damit wir über die Anzahl der abgegebenen und aufgenommenen Elektronen eine Aussage treffen können, müssen wir uns als nächstes mit den Oxidationszahlen beschäftigen.
Die Oxidationszahlen
Mit Hilfe von Oxidationszahlen kann bestimmt werden, welche Elemente innerhalb einer Redoxreaktion Elektronen abgeben oder aufnehmen. Dies lässt sich entweder mit Hilfe der angegeben Regeln oder grafisch bestimmen. Wir beschäftigen uns erstmal nur mit der Anwendung der Regeln. Die Oxidationszahlen werden mit Hilfe von römischen Ziffern angegeben. Diese werden über die Elemente bzw. Verbindungen geschrieben.
Bei den Oxidationszahlen handelt es sich um formale Ladungen. Formale Ladungen existieren nur theoretisch. Oxidationszahlen geben somit an, welche Ladung jedes Atom in einer Verbindung hätte, wenn man die Bindungselektronen dem Bindungspartner mit der höheren Elektronegativität vollständig zuweisen würde.
Formale Ladungen am Beispiel Wasser – Hier Tippen für weitere Infos.
Am Beispiel Wasser lassen sich die formale Ladungen gut erklären. Schauen wir uns die Bindung zwischen dem Wasserstoff- und dem Sauerstoff-Atom (H–O) an. Das Sauerstoff-Atom hat den höheren EN-Wert und somit können die beiden Bindungselektronen dem Sauerstoff-Atom formal vollständig zugeordnet werden.
Das führt dazu, dass das Sauerstoff-Atom zwei Elektronen mehr hätte als im Periodensystem angegeben. Dies führt zu einer formalen Ladung (Oxidationszahl)
von – II.
Während das Wasserstoff-Atom ein Elektron fehlt im Vergleich zu seinem Element im PSE. Somit ergibt sich für das Wasserstoff-Atom eine formale Ladung (Oxidationszahl) von +I.
Die Regeln zum Aufstellen von Oxidationszahlen lauten wie folgt:
Regel gilt nur für Elemente (z.B. O2, Fe)
- Elemente haben immer die Oxidationszahl
Null ± 0.
Folgende Regeln gelten nur für Verbindungen
(z.B. H2O, NH3 , F2O3)
- In einer Verbindung ist die Summe der Oxidationszahlen aller Atome Null ± 0.
- Ein Wasserstoff-Atom hat die Oxidationszahl +I.
- Ein Sauerstoff-Atom hat die Oxidationszahl –II.
- Metalle haben immer eine positive Oxidationszahl.
- Alkalimetalle (1. Hauptgruppe) haben immer die Oxidationszahl +I.
- Erdalkalimetalle (2. Hauptgruppe) haben immer die Oxidationszahl +II.
- In einem Ion ist die Summe der Oxidationszahlen aller Atome gleich der Ionenladung.
- Bearbeite die folgende Präsentation, indem du zu verschiedenen Elementen, Verbindungen und Ionen die Oxidationszahl benennest.
- Vervollständige die Reaktionsgleichungen und gib die Oxidation, Reduktion und die übertragbaren Elektronen an.
- Die beiden Erklärvideos dienen dir als Hilfe zum Aufstellen von Oxidationszahlen und der Anwendung in Reaktionsgleichungen.
In dem Video wird an Beispielen die Bestimmung von Oxidationszahlen erklärt.
In dem Video wird erklärt, wie du die Oxidation und Reduktion in einer Redoxreaktion angeben kannst.
Die Oxidationszahlen von organischen Verbindungen bestimmen (Q-Phase)
In organischen Verbindungen legen wir den Fokus vor allem auf die Kohlenstoff-Atome. Damit wir die Oxidationszahlen bestimmen können, benötigen wir ein Periodensystem mit den Elektronegativitätswerten (EN-Werten). Auf diese Weise können wir nachschauen, wer stärker an den Bindungselektronen in einem Molekül zieht. Die folgende Abbildung zeigt die Elektronegativitätswerte.
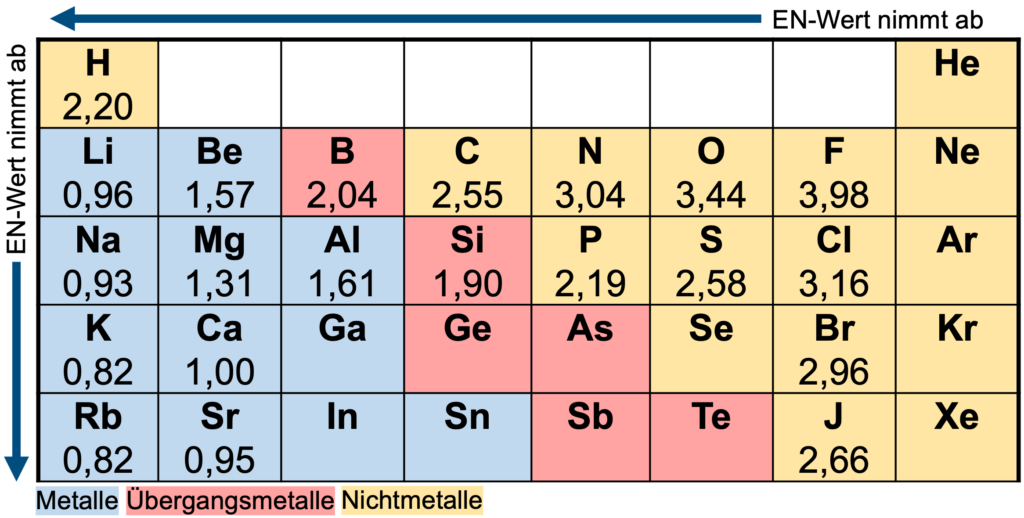
- Schau dir die folgende Präsentation an und bearbeite die darin enthaltene Aufgabe.
Das Wichtigste auf einen Blick