Das Periodensystem der Elemente
Das Periodensystem ordnet die Atome in einer Art chemischen Baukasten, der die Grundlage unserer Welt ist. Aus dem Periodensystem können wir eine Reihe von Informationen z.B. über die Atommasse, die Anzahl der Neutronen oder der Anzahl der Valenzelektronen.
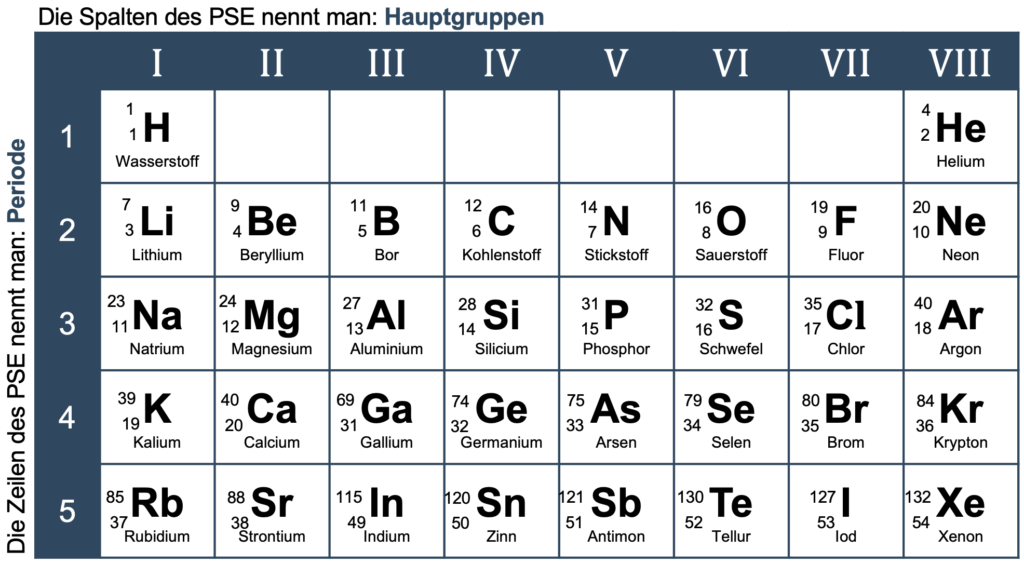
- Vervollständige die Lücken oder wähle die korrekten Aussagen aus. Verwende das Periodensystem als Hilfe.
Im Internet findet man viele verschiedene Periodensysteme. Ich möchte euch ein interaktives und kostenloses von Merck empfehlen. Ihr könnt dieses entweder direkt im Browser z.B. über Safari nutzen oder als App herunterladen.
- Mach dich mit dem Periodensystem von Merck vertraut, indem du dir die Elemente Natrium, Kohlenstoff und Schwefel einmal in der Detailansicht anschaust. Klicke dafür auf das jeweilige Element.
- Wähle in der linken Seite die Kategorie „Aggregatzustand“ aus. Mit Hilfe von dem Schieberegler kannst du die Temperatur einstellen.
- Nenne die kälteste Temperatur die angegeben wird.
- Finde heraus, bei welcher Temperatur die Elemente Wasserstoff und Kohlenstoff fest, flüssig und gasförmig sind.
Die Ionenbindung
Im Periodensystem sind die Elemente einzeln angeordnet. Es besteht die Möglichkeit, dass zwischen den Elementen chemische Bindungen entstehen. Die erste schauen wir uns nun an. Die Ionenbindung kann sich zwischen Metallen und Nichtmetallen ausbilden.
- Schau dir die Präsentation an und bearbeite die dort enthaltenden Aufgaben.
Vertiefung Salze
Es gibt auch andere Salze, die auf den ersten Blick erstmal nicht nach einem klassischen Salz aussehen, aber den Namen in der Bezeichnung tragen. Z.B das Natriumsalz einer Sulfonsäure. Das klingt vielleicht erstmal kompliziert, aber das Salz ist in vielen Shampoos enthalten. Es handelt sich um ein sogenanntes Tensid. Ein Stoff der in Öl und Wasser löslich ist. Aber dazu später mehr.
Zurück zu der Frage, warum spricht man von einem Salz?
Wenn wir uns die Strukturformel anschauen, können wir erkennen, das ein Natrium-Kation vorhanden ist und ein Sauerstoff-Atom, dass eine negative Ladung trägt. Zwischen diesen beiden kann sich somit eine Ionenbindung ausbilden. Es bildet sich zwar kein Ionengitter, aber dennoch spricht man vom Natriumsalz.
Die unpolare Elektronenpaarbindung
Bei der Ionenbindung bilden die Elemente keine Moleküle, da diese Art der Bindung auf Anziehungskräften zwischen den Ionen beruht. Anders ist es bei der Elektronenpaarbindung. In diesem Fall können wir von einem Molekül sprechen, da die einzelnen Elemente ihre Elektronen in einer Bindung teilen.
Im ersten Schritt schauen wir uns die Elektronenpaarbindung im Schalenmodell an.
- Bearbeite die Aufgaben in der Präsentation.
Im zweiten Schritt schauen wir uns an, wie wir die Elektronenpaarbindung mit Hilfe der Valenzstrichformel darstellen können. Dabei liegt der Fokus nur auf den Valenzelektronen eines Atoms. Das Atom Chlor hat 7 Valenzelektronen. Aber es ist jeweils nur ein Elektron an der Bindung beteiligt. Die übrigen Valenzelektronen, die nicht an Bindungen beteiligt sind, werden als Punkte oder als Striche neben die Atomsymbole geschrieben, wobei ein Strich immer für ein Elektronenpaar steht. Diese Strichformeln werden auch Lewis-Formeln genannt. Die Theorie von Lewis betont das Erreichen der Oktettregel als Ziel für jedes Atom.
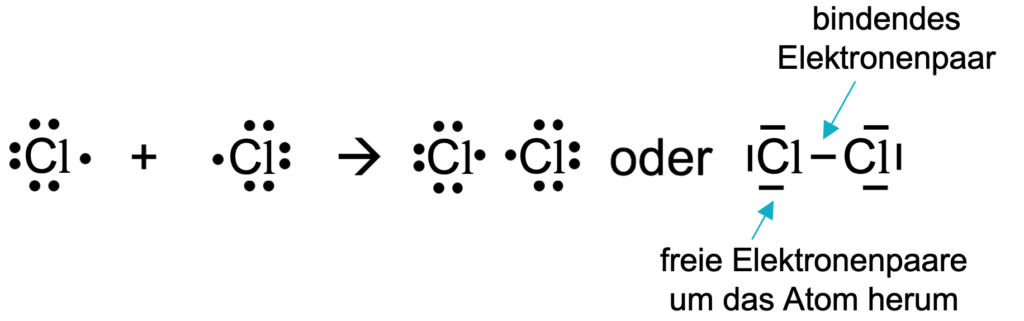
In dem folgenden Ausschnitt aus dem Periodensystem sind zu ausgewählten Elementen bindende Elektronen und freie Elektronenpaare angegeben. Diese Darstellung hilft dir dabei, Moleküle korrekt zusammenzusetzen, indem du alle bindenden Elektronen in einem Molekül verwenden musst, um die Oktettregel zu erreichen.
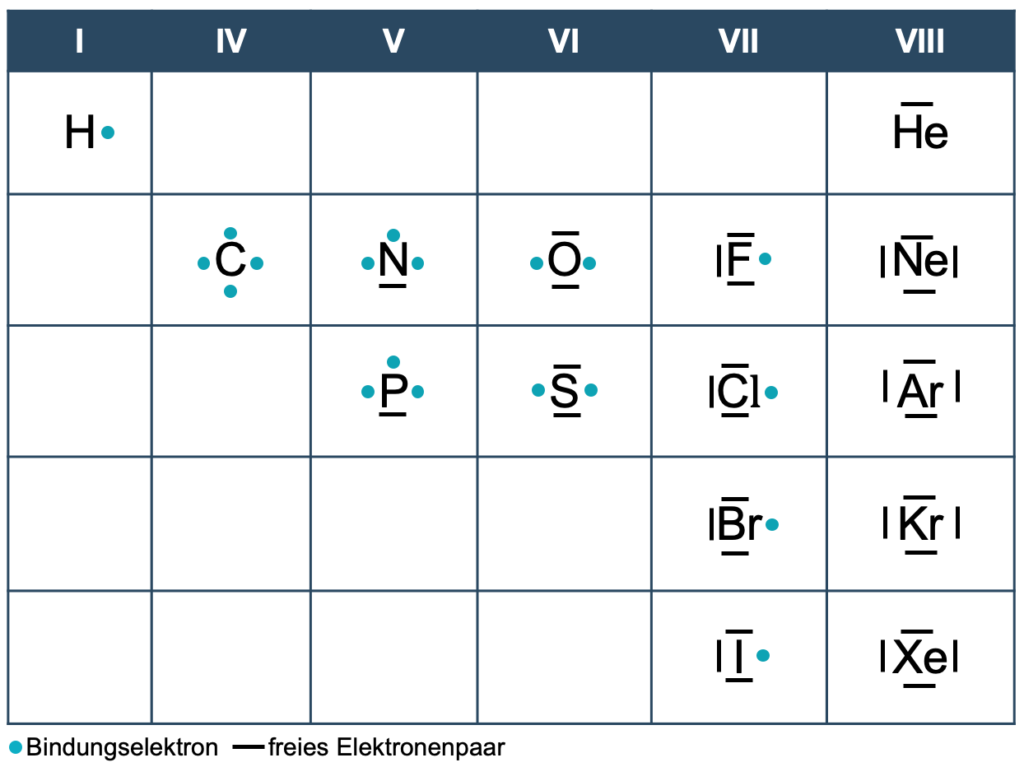
- Übe nun, die Valenzstrichformel anzuwenden. Verwende als Hilfe die Tabelle 1.
Vertiefung – Ausnahme von der Oktettregel ab der 3. Periode
Ab der 3. Periode gibt es Ausnahmen von der Oktettregel und es können auch mehr Bindungselektronen für die Bildung von Molekülen verwendet werden. Deutlich wird dies am Phosphor- (P) und Schwefel (S) -Atom in der folgenden Abbildung. Wie viele Valenz-elektronen für Bindungen verwendet werden, hängt von dem zu bildenden Molekül ab.

Das Phosphat-Atom im Monophosphan erfüllt die Oktettregel, indem drei bindende Elektronen für eine Elektronenpaarbindung verwendet werden. Zusammen mit dem freien Elektronenpaar verfügt das Phosphat-Atom über 8 Valenzelektronen.
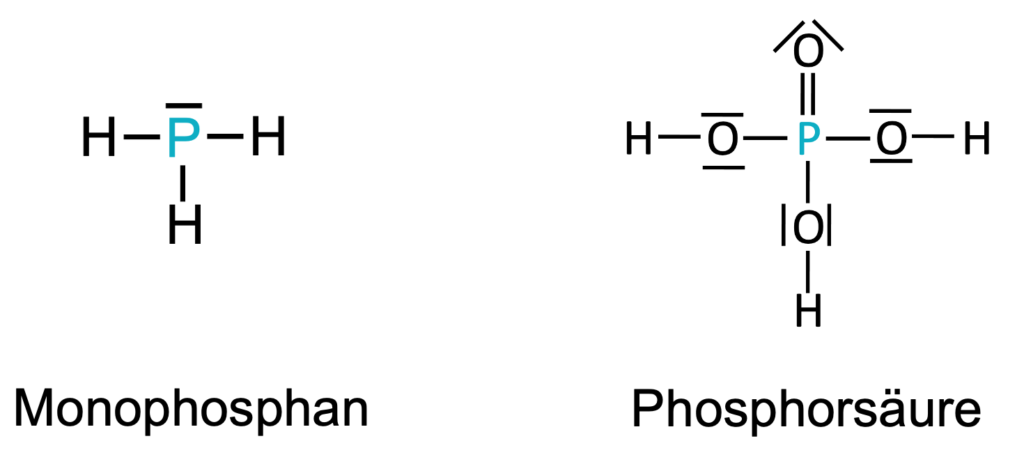
Die Phosphat-Atom in der Phosphorsäure hingegen verwendet alle Valenzelektronen für Elektronenpaarbindungen und übersteigt damit die Oktettregel und verfügt über 10 Valenzelektronen und ist trotzdem stabil. Dieser Molekülaufbau lässt sich nur mit dem Orbital-Modell erklären. Das geht an dieser Stelle jedoch zu weit.
Du musst dich also in Zukunft nicht wundern, falls dir Moleküle begegnen, die die Oktettregel nicht erfüllen. Weitere Ausnahmen sind bei Chlor (Cl), Brom (Br) und Iod (I) möglich.
Die polare Elektronenpaarbindung
Wir habe nun verstanden, wie eine Elektronenpaarbindung zustande kommt. Dir ist aber sicher aufgefallen, dass bereits eine Unterscheidung in eine unpolare und polare Elektronenpaarbindung getroffen wurde. Den Unterschied wollen wir uns nun etwas genauer anschauen.
- Schau dir das Video an und beschreibe deine Beobachtungen.
- Wenn noch Zeit ist, kannst du den Versuch mit dem Wasserstrahl im Unterricht ausprobieren.
- Lies das Arbeitsmaterial zu den polaren Elektronenpaarbindungen.
Bei einem Wasser-Molekül handelt es sich um einen Dipol, da sich die Elektronen in den Bindungen verschieben. Damit handelt es sich im Wasser-Molekül um eine polare Elektronenpaarbindung. Wir lernen nun, wie sich die Bindungsart ermitteln lässt!
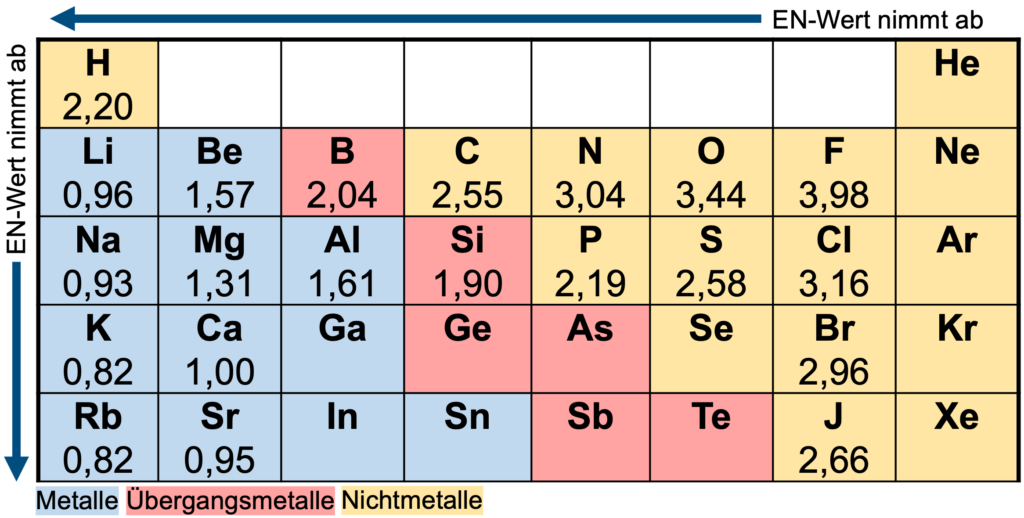
Das folgende Periodensystem zeigt dir die Elektronegativitätswerte für einige Elemente. Die Elektronegativität beschreibt die Fähigkeit eines Atoms, innerhalb eines Moleküls von benachbarten Atomen die Bindungselektronen anzuziehen. Den größten EN-Wert hat Fluor (F) mit 3,98. Im nächsten Schritt berechnen wir die Elektronegativitäts-Differenzen (oder kurz: ΔEN) zwischen zwei Elementen, um die Bindungsart zu bestimmen.
Beispiel: Der EN-Wert von Sauerstoff ist 3,44 und der von Wasserstoff ist 2,20. Die Differenz aus den beiden Werten ist also 3,44 – 2,20 = 1,24. ΔEN = 1,24
ΔEN größer als 1,7: Ionenbindung
ΔEN zwischen 0,4 – 1,7: polare Elektronenpaarbindung
ΔEN kleiner als 0,4:
unpolare Elektronenpaarbdg.
- Bearbeite die Aufgaben in der Präsentation.
Vertiefung – Nicht jede polare Bindung führt zu einem polarem Molekül
Nicht jedes Molekül, dass polare Elektronenpaarbindungen besitzt ist auch ein polares Molekül. Die Voraussetzung für ein polares Molekül ist ein Dipol!
Ob ein Dipol entsteht, ist abhängig von der Symmetrie des Moleküls. Das Wasser-Molekül ist gewinkelt und dies führt dazu, dass die Elektronendichte innerhalb des Moleküls asymmetrisch (ungleichmäßig) verteilt ist. Bei dem CO2-Molekül ist das anders. Trotz der partiell positiven und negativen Ladungen ist das Molekül unpolar.
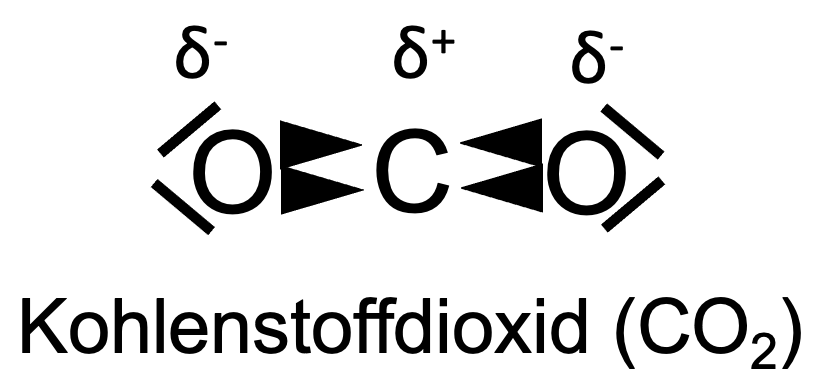
Das liegt an der Symmetrie des CO2-Moleküls. Das Molekül ist linear und das führt dazu, dass sich die drei Partialladungen aufheben.
Das Chlorwasserstoff-Molekül (HCl) ist auch linear, aber verfügt nur über eine partiell positive und negative Ladung. Damit ist die Elektronendichte innerhalb des Moleküls asymmetrisch verteilt und es bildet sich ein Dipol.
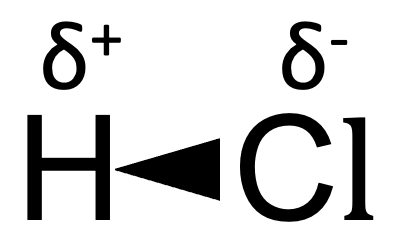
Merke dir also, dass dass neben der polaren Bindung auch die Symmetrie des Moleküls eine Rolle spielt.
Die Metallbindung
Die letzte Bindungsart die wir uns anschauen wollen betrifft nur die Metalle im Periodensystem. Der Aufbau von einem Metall lässt sich in einen Atomrumpf und ein Elektronengas unterteilen (siehe Abbildung). Die Außenelektronen von einem Metallatom sind nicht mehr einem einzelnen Atom zugeordnet, sondern können sich im gesamten Metallgitter freibewegen. Dieses bezeichnet man als Elektronengas. Die einzelnen positiv geladenen Metallionen (in unserem Beispiel Na+) bilden ein geordnetes Gitter. Die einzelnen Metallatome werden als Atomrumpf bezeichnet, damit beschreibt man ein Atom ohne Außenelektronen.
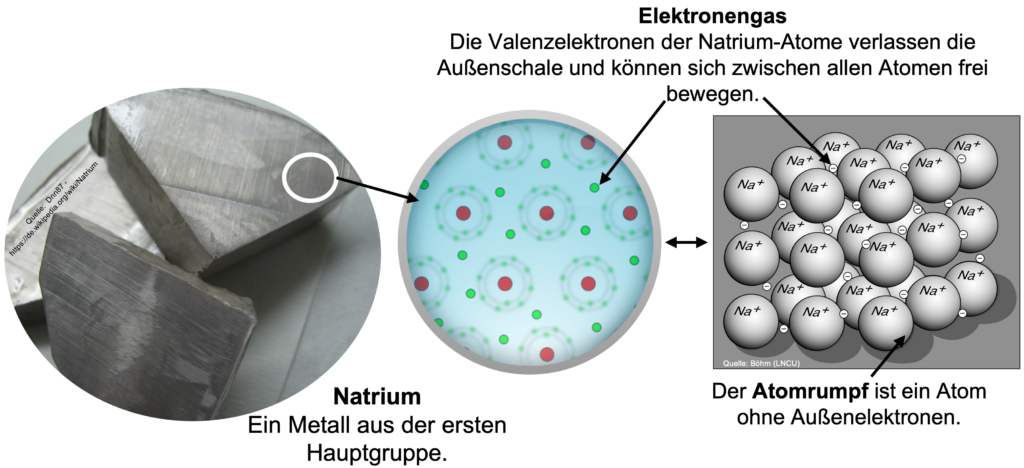
Metalle weisen unterschiedliche Eigenschaften auf, die dir vielleicht schon im Alltag aufgefallen sind:
- Sie leiten Wärme (Wärmeleitfähigkeit).
- Sie leiten Strom (elektrische Leitfähigkeit).
- Sie lassen sich verformen (Verformbarkeit).
- Sie glänzen im Licht (metallischer Glanz).
- Schaue dir das folgende Video zu den Metallbindungen an.
- Beschreibe mit deinen eigenen Worten den Aufbau von dem Metall Natrium, indem du dich auf die Abbildung 1 beziehst.
- Erläutere, wie die oben aufgeführten Eigenschaften der Metalle zustande kommen.
- Wir vergleichen die Antworten gemeinsam im Unterricht.
Das Wichtigste auf einen Blick