Zwischenmolekulare Wechselwirkungen
Es existieren eine Reihe verschiedener zwischenmolekularer Wechselwirkungen. Du fragst dich vielleicht, warum es wichtig ist, diese zu kennen. Aber mach dir bewusst, dass unsere Welt voller unterschiedlichster Moleküle ist. Ständig treten diese in Wechselwirkungen zueinander und beeinflussen sich so gegenseitig.
Bei den zwischenmolekularen Wechselwirkungen handelt es sich nicht um Bindungen, wie die Elektronenpaarbindung oder die Ionenbindung, sondern um schwache Wechselwirkungen zwischen Molekülen, die auf Grund von gegensätzlichen partiellen Ladungen entstehen.
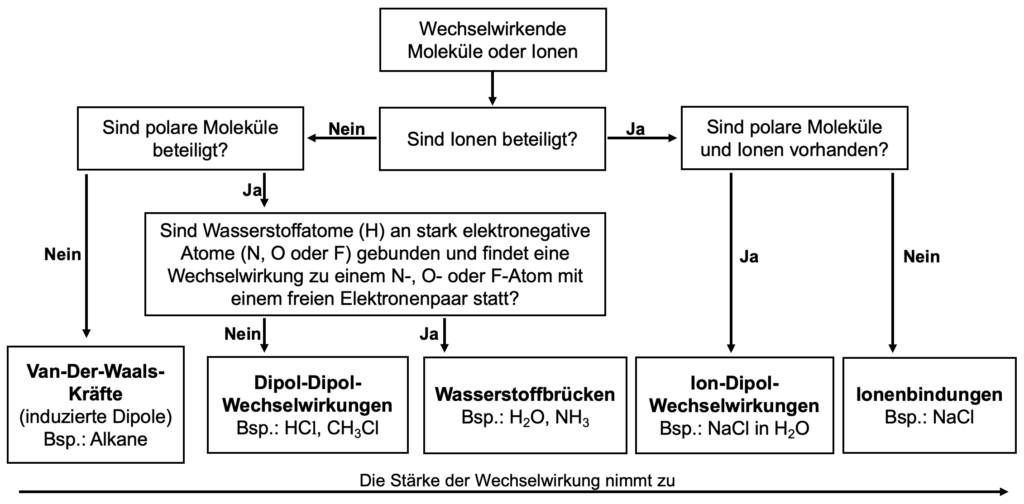
Mit Hilfe der Abbildung 1 können wir herausfinden, welche Wechselwirkung sich zwischen verschiedenen Molekülen bilden können, indem du dir die Struktur des Moleküls anschaust und die folgenden Fragen beantwortest.
Wasserstoffbrücken und Dipol-Dipol-Wechselwirkungen
Im ersten Schritt schauen wir uns zwischenmolekulare Wechselwirkungen an, die zwischen polaren Molekülen entstehen. Polare Moleküle zeichnen sich dadurch aus, dass es im Molekül zu einer dauerhaften Ladungsverschiebung kommt und sich polare Bindungen bilden. Die Ladungsverschiebung entsteht durch unterschiedlich starke Elektronegativitätswerte zwischen den Atomen im Molekül. Im Salzsäure-Molekül zieht das Cl-Atom stärker an den Bindungelektronen als das Wasserstoff-Atom. Diese Ladungsverschiebung wird mit einem Keil dargestellt.
Du kannst aus der Abbildung 1 ableiten, dass sich sowohl Wasserstoffbrücken als auch Dipol-Dipol-Wechselwirkungen zwischen polaren Molekülen ausbilden. Die beiden Wechselwirkungen lassen sich unterscheiden, indem man überprüft an welche Atome die Wasserstoffatome gebunden sind und mit welchen Atomen diese wechselwirken.
Wasser ein polares Molekül

Chlorwasserstoff ein polares Molekül
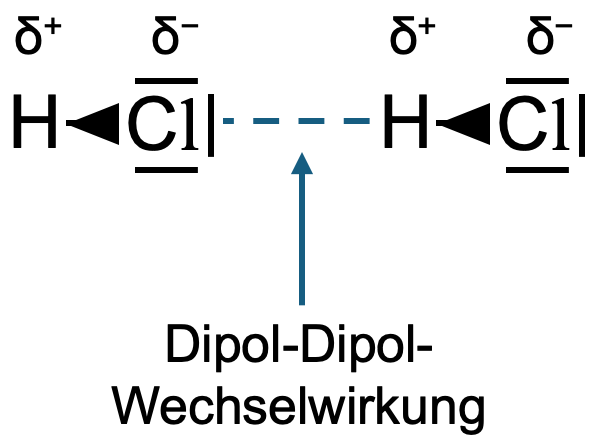
Eine Wasserstoffbrücke lässt sich daran erkennen, dass Wasserstoffatome (H) an stark elektronegative Atome (N, O oder F) gebunden sind und eine Wechselwirkung zu einem N-, O- oder F-Atom mit einem freien Elektronenpaar ausbilden. Treffen diese beiden Bedingungen nicht zu, dann handelt es sich um eine Dipol-Dipol-Wechselwirkung wie bei den Chlorwasserstoff-Molekülen.
- In der folgenden Präsentation wirst du verschiedene Moleküle-Ausschnitte gezeigt bekommen. Übertrage diese in deine Unterlagen.
- Ergänze polare Elektronenpaarbindungen mit einem Keil, freie Elektronenpaare und benenne die zwischenmolekulare Wechselwirkung (gestrichelte Linie).
Vertiefung – Die Oberflächenspannung von Wasser
Zur Erinnerung: Durch die Wasserstoffbrücken zwischen den einzelnen Wassermolekülen, kann an der Oberfläche von Wasser (Grenzfläche Wasser & Luft) eine Oberflächenspannung entstehen, da zur Luft keine Wasserstoffbrücken ausgebildet werden können. Auf dieser Oberflächenspannung kann sich ein Wasserläufer bewegen oder eine Büroklammer schwimmen ohne unterzugehen.

Wasser als Lösungsmittel
Wasser wird gerne als Lösungsmittel verwendet, um andere Stoffe darin aufzulösen. Damit ein Stoff sich gut in einem anderen Stoff löst, müssen zwischen den Stoffen zwischenmolekulare Wechselwirkungen ausgebildet werden. Je mehr Wechselwirkungen vorhanden sind, desto besser ist das Löseverhalten. Schauen wir uns das ganze am Beispiel Zucker (Glucose) an.
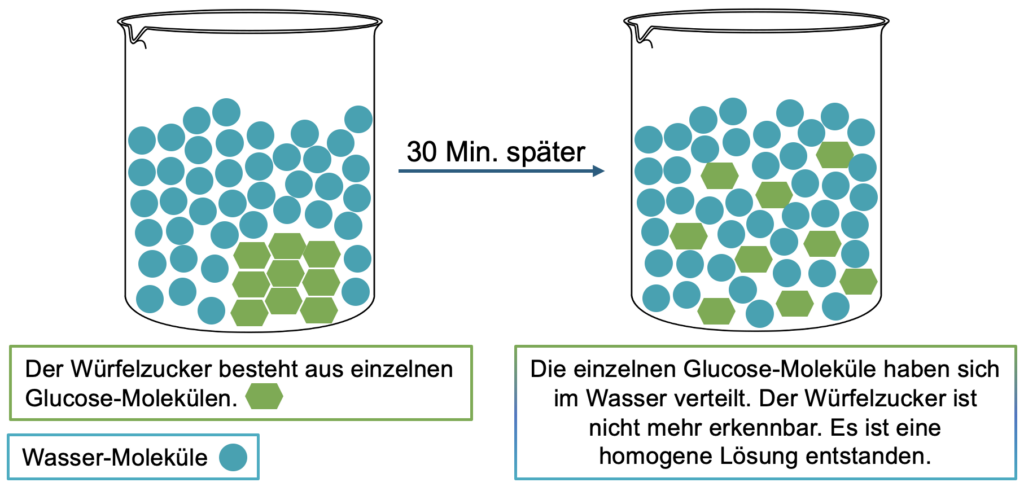
In einem Becherglas befindet sich zu Beginn ein Stück Würfelzucker, der sich im Laufe der Zeit auflöst. Dabei verteilen sich die einzelnen Glucose-Moleküle vollständig im Wasser.
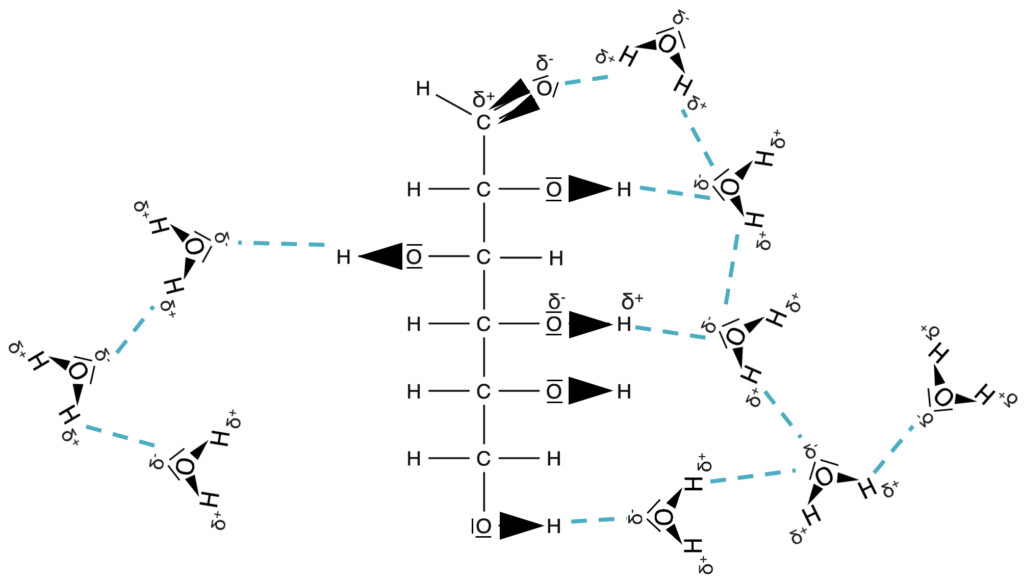
Im nächsten Schritt legen wir den Fokus auf ein Glucose-Molekül und die Wechselwirkungen mit den Wasser-Molekülen. Die folgende Abbildung zeigt in der Mitte ein Glucose-Molekül. Die polaren Elektronenpaarbindungen in den O-H-Gruppen wurden bereits mit einem Keil dargestellt. Es wird deutlich, dass mehrere Dipole im Molekül vorhanden sind. Diese können mit den Wasser-Molekülen Wasserstoffbrücken ausbilden.
Es kann übrigens nicht unendlich viel Glucose im Wasser gelöst werden. Ab einer bestimmten Menge setzt sich Glucose als ungelöster Feststoff am Boden des Glases ab. Sobald dieses zu beobachten ist, spricht man von einer gesättigten Lösung. Dies lässt sich damit erklären, dass nicht mehr ausreichend Wasser-Moleküle vorhanden sind, um mit allen Glucose-Molekülen Wasserstoffbrücken ausbilden zu können.
Lösen von Salz in Wasser – die Ion-Dipol-Wechselwirkung
Ein weiteres Beispiel ist das auflösen von Salz in Wasser. Wie wir bereits wissen, bestehen Salze aus Anionen und Kationen und bilden ein Ionengitter. Wird Salz in Wasser gegeben, lagern sich die Wasser-Moleküle um das Ionengitter und lösen die einzelnen Ionen heraus. Die einzelnen Ionen werden von mehreren Wassermolekülen umgeben. Diese Umlagerung wird als Hydrathülle bezeichnet. Zwischen den Ionen und den Wassermolekülen bilden sich Ion-Dipol-Wechselwirkungen. Die zahlreichen Wechselwirkungen führen zu einer guten Lösbarkeit der Salze im Wasser.
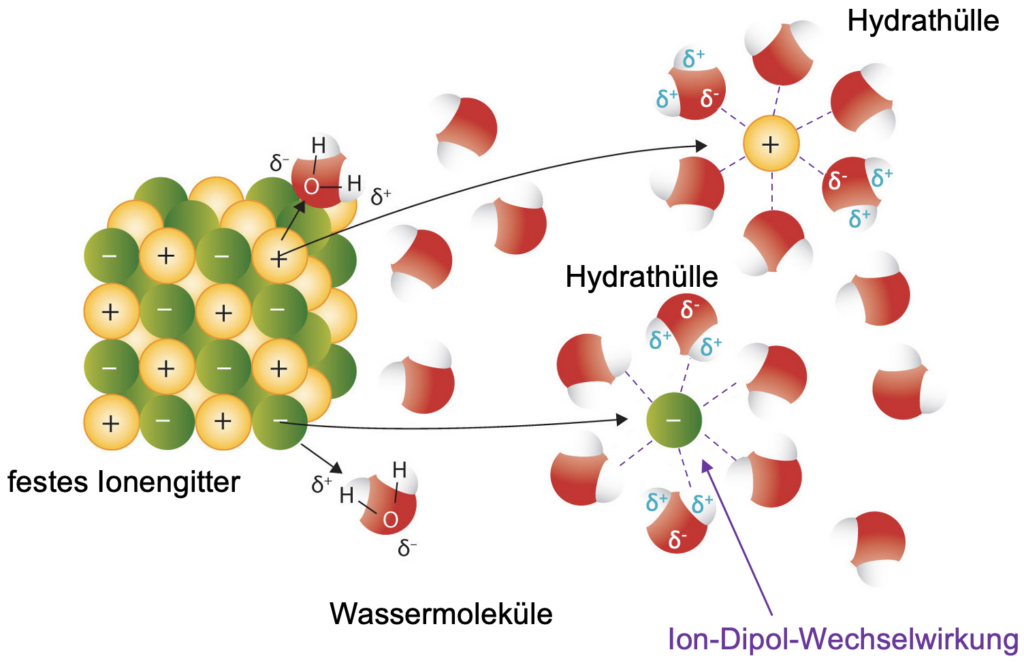
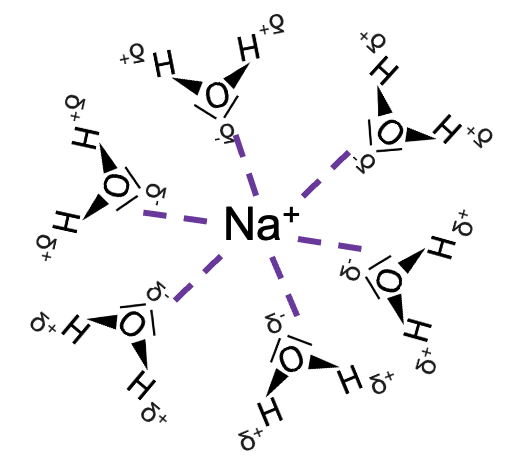
Du wirst in Zukunft auch noch andere Moleküle kennenlernen. Dabei wirst du feststellen, dass ein Molekül je nach Aufbau auch mehrere verschiedene Wechselwirkungen ausbilden kann. Je mehr Wechselwirkungen mit dem Lösungsmittel wie Wasser ausgebildet werden kann, desto besser löst sich der Stoff.
Die Van-der-Waals-Kräfte
Wir habe nun viel über Wasser gesprochen, aber es gibt auch noch andere Flüssigkeiten, die andere Eigenschaften aufweisen wie z.B. Heptan. Zwischen den Heptan-Molekülen bilden sich Van-der-Waals-Kräfte, dabei handelt es sich um die schwächsten zwischenmolekularen Wechselwirkungen. Diese können zwischen unpolaren Molekülen entstehen, indem sich kurzzeitige (temporäre) Dipole bilden. Die Kräfte existieren nur für ein paar millionstel Sekunden. Allerdings können sich diese Anziehungskräfte immer wieder an verschiedenen Stellen im Molekül neu bilden.
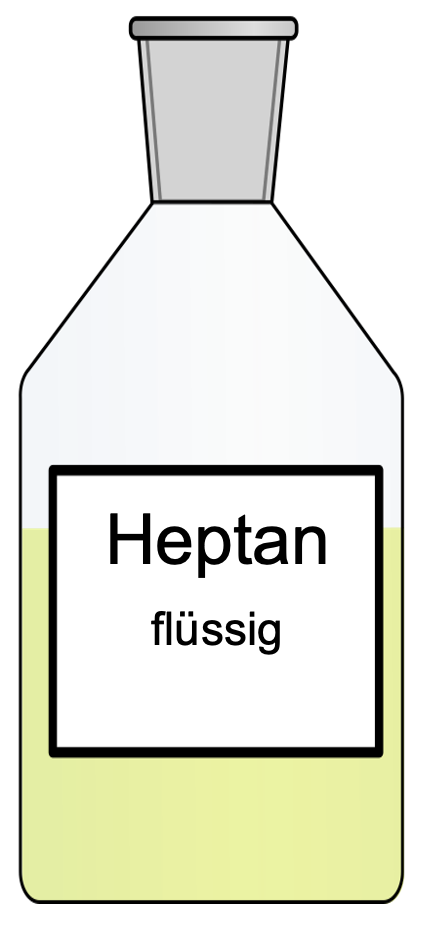
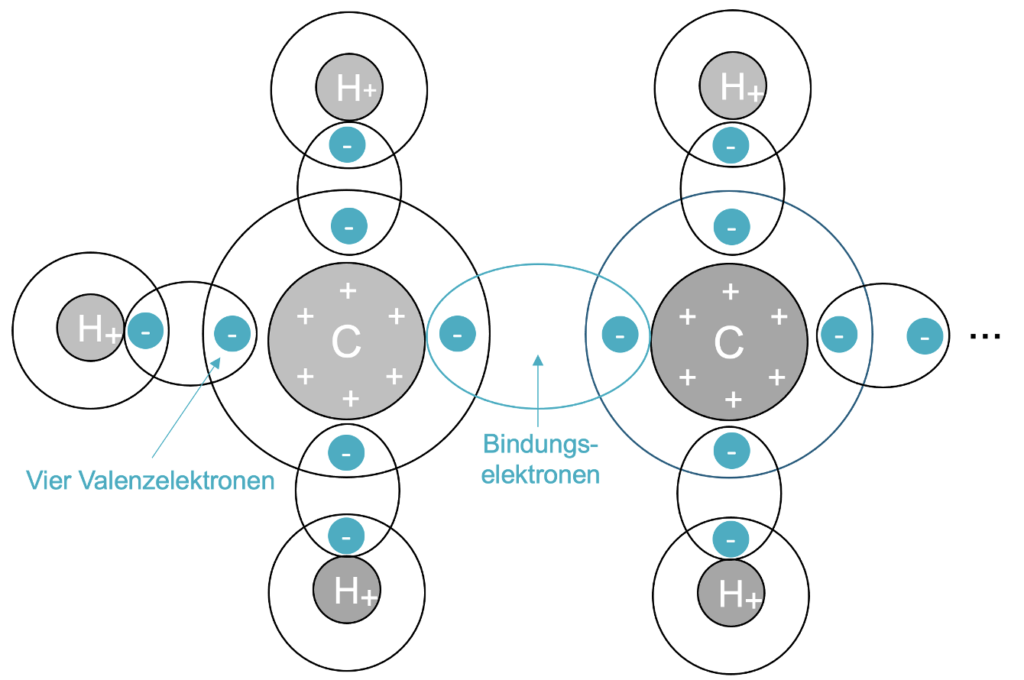
Dargestellt ist ein Heptan-Molekül. Dabei handelt es sich um ein unpolares Molekül. Es werden die Van-der-Waals-Kräfte angedeutet. Um die Entstehung der Kräfte zu verstehen, müssen wir uns den Molekülaufbau im Schalenmodell anschauen.
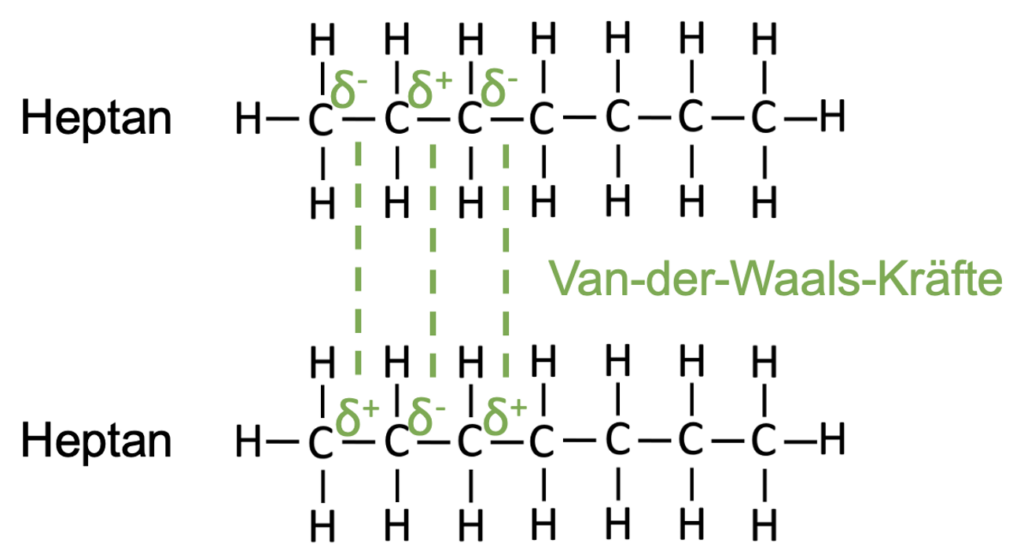
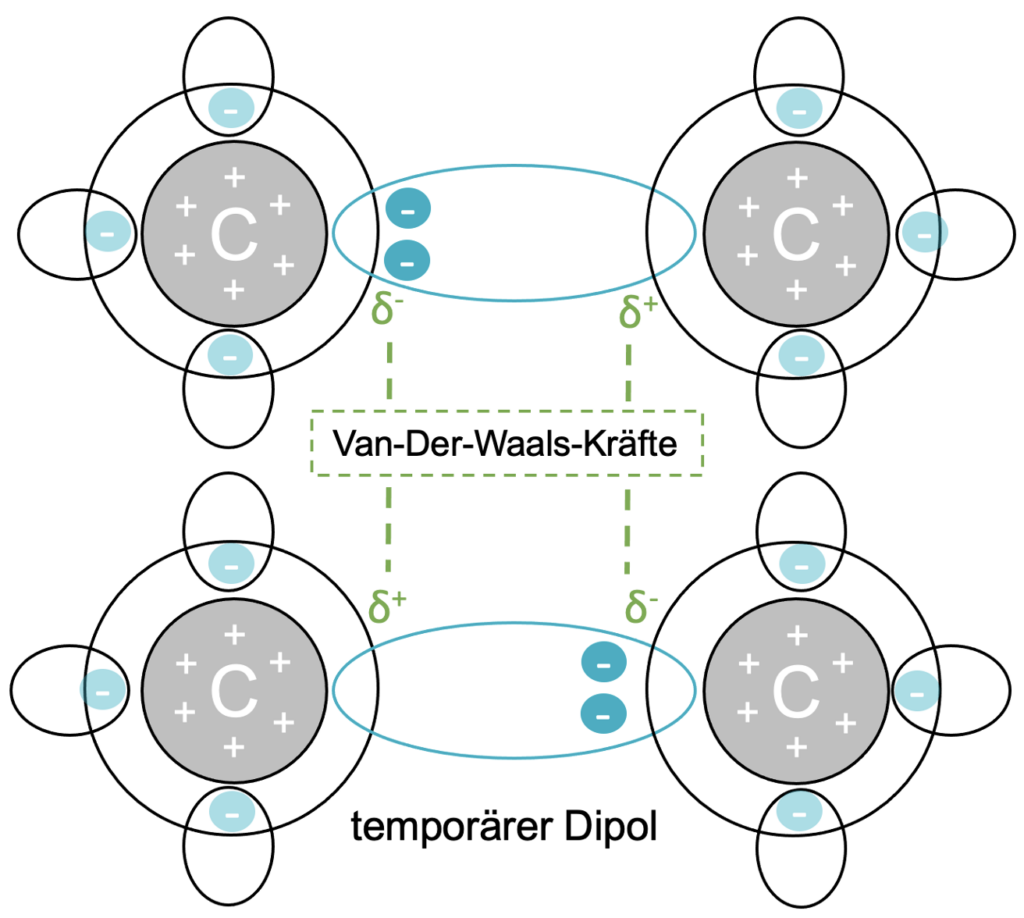
Die folgenden beiden Abbildungen zeigen die kurzzeitige Entstehung der Van-der-Waals-Kräfte. Dabei handelt es sich einen Ausschnitt aus dem Heptan-Molekül (zwei C-Atome zu Beginn der Kette). Die Elektronen in einer Elektronenpaarbindung sind ständig in Bewegung und so kann es zufällig passieren, dass sich Elektronen vermehrt auf einer Seite aufhalten.
Dieses führt zu einer Ladungsverschiebung, die dafür sorgt, dass in einem Teil des Moleküls ein partiell negativer (δ–) und partiell positiver Bereich (δ+) entsteht. Dieser Zustand ist nur von kurzer Dauer und wird als temporärer Dipol bezeichnet. Dieser temporärer Dipol kann bei einem benachbartem Molekül ebenfalls einen Dipol erzeugen. Da diese Kräfte nun gegensätzlich sind, können sich kurzzeitige Anziehungskräfte ausbilden, die als Van-der-Waals-Kräfte bezeichnet werden. Die Kräfte können nur so lange bestehen, bis sich die Elektronen wieder symmetrisch verteilt haben.
- Recherchiere im Internet, welchen Zusammenhang es zwischen einem Gecko und den Van-der-Waals-Kräfte gibt.
- Du hast nun zahlreiche Wechselwirkungen kennengelernt. Schau dir in der folgenden Präsentation die verschiedenen Moleküle an und benenne die zwischenmolekulare Wechselwirkung (gestrichelte Linie).
Mischen von polaren und unpolaren Flüssigkeiten
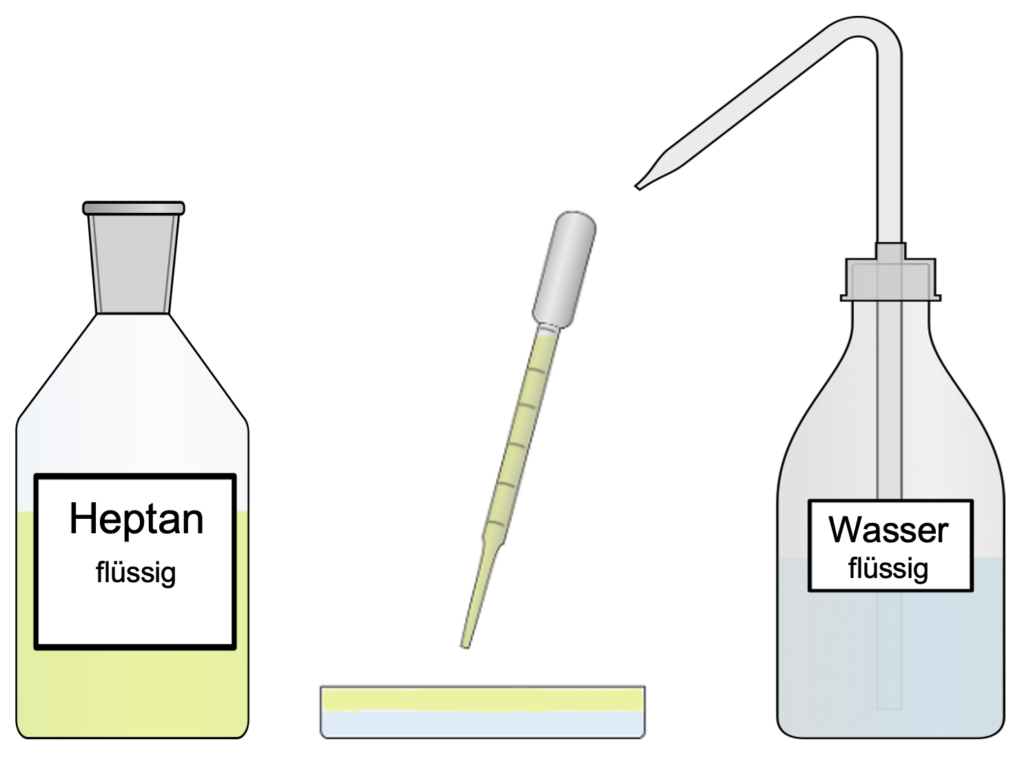
Als nächstes Mischen wir die beiden Flüssigkeiten Heptan und Wasser und können erkennen, dass sich zwei Phasen bilden. Die untere Phase besteht aus Wasser, während die obere Phase aus Heptan besteht. Es kommt somit zu keiner Durchmischung der beiden Stoffe. Diese Beobachtung können wir erklären, wenn wir auf die Teilchenebene wechseln und uns die Moleküle nochmal anschauen.
Merksatz:
Gleiches löst sich in gleichem!
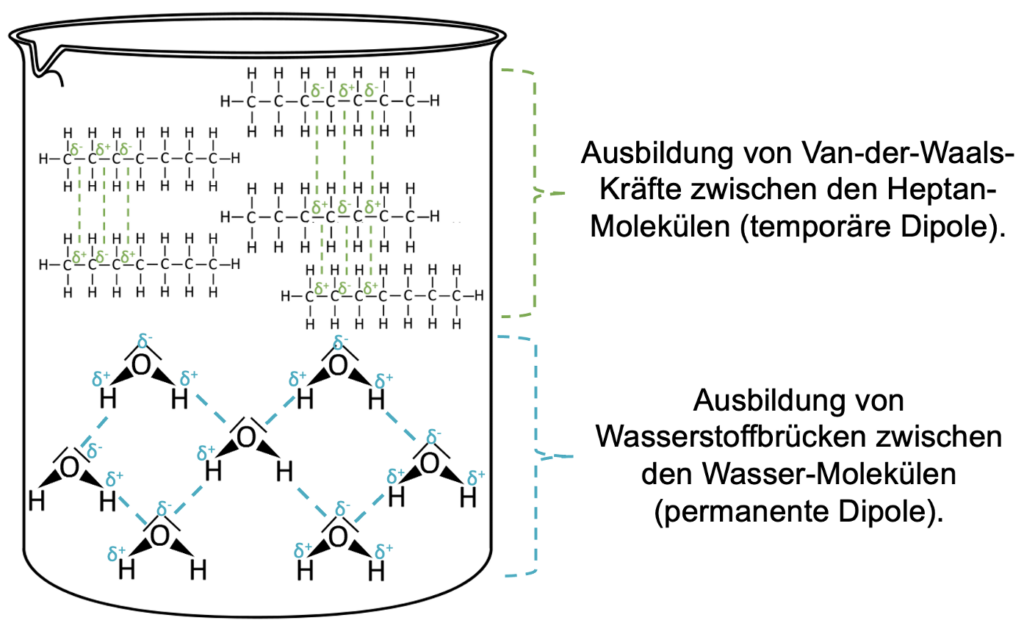
Den hervorgehobenen Merksatz musst du dir unbedingt merken. Dieser bezieht sich auf die zwischenmolekularen Wechselwirkungen. Es wird damit zum Ausdruck gebracht, dass sich Moleküle, die untereinander Wechselwirkungen ausbilden können, sich auch ineinander lösen bzw. mischen können. In diesem Fall können Wasser-Moleküle untereinander Wasserstoffbrücken bilden und Heptan-Moleküle können untereinander Van-der-Waals-Kräfte bilden, aber es gibt keine zwischenmolekularen Wechselwirkungen zwischen den Wasser- und Heptan-Molekülen.
- In der nächsten Übung werden dir verschiedene Stoffe vorgegeben. Diese werden in Wasser als auch in Heptan gegeben. Begründe, ob sich der Stoff in Wasser und/oder Heptan lösen kann.
- Die folgenden Schritte können dir bei der Bearbeitung der Aufgabe helfen.
Vorgehen, um die Löslichkeit von Molekülen bewerten zu können.
- Analysiere die Molekülstrukturen und überprüfe, welche Bindungsarten (polare Bindung, unpolare Bindung und Ionenbindung) vorliegen. Es können auch mehrere Bindungsarten in einem Molekül vorhanden sein.
- Prüfe, ob und welche zwischenmolekularen Wechselwirkungen sich zu dem Lösungsmittel ausbilden können.
- Formuliere eine Begründung zur Löslichkeit.
Erklärvideo zu den Bindungsarten und Wechselwirkungen
Das Wissen über die verschiedenen Arten von Bindungen und die zwischenmolekularen Wechselwirkungen sind eng miteinander verknüpft. Es handelt sich dabei um wichtige Grundkenntnisse der Chemie. Aus diesem Grund habe ich die wichtigsten Inhalte noch einmal in einem Erklärvideo für euch zusammengefasst.
- Schaue dir das Erklärvideo an.
- Überprüfe dein Wissen, indem du die interaktive Übung im Lernbaustein „Periodensystem und Bindungsarten“ absolvierst:
- Überprüfe dein Wissen, indem du die interaktive Übungen im Lernbaustein „Wechselwirkungen und Löslichkeit“ absolvierst:
- Link direkt zur Übung 1
- Link direkt zur Übung 2
- Link direkt zur Übung 3
- Das wichtigste auf einen Blick – Übung 4
Das Wichtigste auf einen Blick